
CaMKII (Calmodulin Bağımlı Protein Kinaz II), hücre biyolojisinde önemli roller üstlenen ve özellikle sinir hücrelerinde etkili bir protein kinazdır. Protein kinazlar, proteinlerin fosforilasyonu yoluyla biyolojik süreçleri düzenleyen enzimlerdir. CaMKII’nin önemi, sinir sistemi başta olmak üzere çeşitli hücre türlerinde sinyal iletimini düzenlemesinden kaynaklanır. Beyindeki hafıza ve öğrenme süreçlerinden, kalp ritminin düzenlenmesine kadar geniş bir yelpazede işlevi vardır. Bu yazıda, CaMKII molekülünün yapısını, işlevlerini ve biyolojik süreçlerdeki kritik rolünü inceleyeceğiz.
CaMKII Molekülünün Yapısı ve Aktivasyonu
CaMKII, çok alt birimli bir enzim kompleksidir ve dört izoformu bulunur: alfa, beta, gama ve delta. Bu izoformlar farklı dokularda ifade edilerek, CaMKII’nin çok yönlü işlevlerini yerine getirmesine olanak sağlar. Özellikle CaMKII-alfa izoformu beyinde yoğun olarak bulunur ve sinaptik plastisite, öğrenme ve hafıza süreçlerinde kritik rol oynar.
CaMKII’nin aktivasyonu, kalsiyum iyonlarının (Ca²+) calmodulin adlı bir proteinle bağlanmasıyla gerçekleşir. Calmodulin, Ca²+ seviyelerindeki artışla aktif hale gelir ve CaMKII’ye bağlanarak enzim aktivasyonunu başlatır. CaMKII’nin fosforilasyonu ile aktive olması, proteinlerin yapısal ve işlevsel özelliklerinde kalıcı değişikliklere yol açar. Bu özellik, CaMKII’nin sinaptik plastisiteyi destekleyen temel bir mekanizma olarak görev yapmasını sağlar.
Sinaptik Plastisite ve Öğrenme Üzerindeki Rolü
Beyin hücreleri arasındaki iletişim sinaps adı verilen yapılar aracılığıyla gerçekleşir. Sinapslar, nöronlar arasında bilgi iletimini sağlayan bağlantılardır. Sinaptik plastisite, bu sinapsların işlevselliğinin değiştirilebilmesi anlamına gelir ve öğrenme, hafıza gibi bilişsel süreçlerin temelini oluşturur. CaMKII, bu plastisiteyi sağlayan önemli proteinlerden biridir.
LTP (Uzun Süreli Potansiyasyon)
CaMKII, özellikle uzun süreli potansiyasyon (LTP) adlı sinaptik plastisite sürecinde merkezi bir rol oynar. LTP, sinapsların güçlenmesine yol açan bir mekanizmadır ve öğrenme ve hafızanın biyokimyasal temelidir. Bu süreç, bir sinapsa tekrarlayan uyarılar geldiğinde, bu sinapsın daha güçlü hale gelmesi anlamına gelir. CaMKII, LTP sürecinde AMPA reseptörlerinin sinapsa eklenmesine yardımcı olur ve bu sayede sinaptik iletimin güçlenmesini sağlar. LTP’nin başarısı, CaMKII’nin uygun şekilde fosforile edilmesi ve sinapslarda aktif kalması ile doğrudan ilişkilidir.
CaMKII’nin sinaptik plastisitedeki rolü, öğrenme ve hafıza süreçleri üzerinde derin bir etkiye sahiptir. Özellikle deneysel çalışmalarda, CaMKII aktivitesinin bozunmasının öğrenme yeteneğini olumsuz etkilediği gösterilmiştir. Bununla birlikte, CaMKII aktivitesinin normalin üzerine çıkmasının da aşırı uyarılma ile ilişkili nörolojik bozukluklara yol açabileceği düşünülmektedir.
CaMKII ve Nörolojik Hastalıklar
CaMKII’nin sinaptik plastisitedeki kritik rolü, çeşitli nörolojik hastalıklarda da bu molekülün önemini gündeme getirmiştir. Alzheimer hastalığı, epilepsi ve depresyon gibi nörolojik bozukluklarda CaMKII işlev bozukluğunun rol oynadığı bilinmektedir.
Alzheimer Hastalığı
Alzheimer hastalığı, beyinde bellek ve bilişsel işlevlerin kaybıyla karakterize edilen bir nörodejeneratif hastalıktır. CaMKII, Alzheimer hastalarında sinaptik iletimdeki bozulmalarla ilişkilendirilmiştir. Beyindeki sinaptik bağlantıların kaybı, hastalığın erken evrelerinde bile gözlenir ve bu da CaMKII’nin plastisiteyi sürdürme işlevinde sorunlara yol açar. Alzheimer hastalığının bir diğer belirgin özelliği olan amiloid-beta plaklarının birikimi, CaMKII aktivitesini bozarak sinaptik fonksiyonların daha da kötüleşmesine sebep olabilir.
Epilepsi
Epilepsi, anormal nöronal aktivite sonucu tekrarlayan nöbetlerle karakterize edilen bir hastalıktır. CaMKII’nin bu hastalıktaki rolü, aşırı sinaptik uyarılabilirliğin düzenlenmesinde ortaya çıkar. CaMKII’nin hiperaktivitesi, sinaptik iletimi aşırı derecede artırarak nöbetlerin ortaya çıkmasına katkıda bulunabilir. Epilepsi tedavisinde, CaMKII’nin bu aşırı aktivitesini düzenlemeyi hedefleyen terapiler üzerinde çalışmalar yapılmaktadır.
Depresyon
Depresyon, karmaşık ve çok faktörlü bir psikiyatrik bozukluktur. CaMKII, sinaptik plastisite ve beyindeki nörotransmitter dengesinin korunmasında kritik bir rol oynadığı için depresyonla da ilişkilendirilmiştir. Depresif hastalarda CaMKII’nin işlev bozukluğu, sinaptik bağlantıların zayıflamasına ve bu durumun duygudurum düzenlemesi üzerinde olumsuz etkilere yol açmasına neden olabilir. Bu nedenle, CaMKII aktivitesini modüle eden tedavi yaklaşımları depresyon tedavisinde potansiyel bir hedef olarak incelenmektedir.
CaMKII’nin Diğer Biyolojik Fonksiyonları
CaMKII, yalnızca beyinde değil, kalp, kas ve diğer organlarda da işlev göstermektedir. Özellikle kardiyovasküler sistemde, CaMKII’nin kalp ritmi ve kasılma gücü üzerindeki etkisi önemlidir. Kalp kasında, CaMKII’nin aşırı aktivasyonu aritmi ve kalp yetmezliği gibi ciddi kardiyak sorunlara yol açabilir. Bu nedenle, CaMKII’nin kardiyovasküler sistemdeki düzenleyici rolü, kalp hastalıkları araştırmalarında önemli bir odak noktasıdır.
Kalp Fonksiyonu
CaMKII, kalp hücrelerinde kalsiyum sinyallerinin düzenlenmesinde görev alır. Kalbin kasılma ve gevşeme döngüsünde kalsiyumun rolü büyük olduğundan, CaMKII’nin bu süreci düzenlemesi hayati bir öneme sahiptir. Ancak CaMKII’nin aşırı aktivasyonu, hücresel stres tepkilerini tetikleyebilir ve kalp yetmezliği gibi durumların ortaya çıkmasına neden olabilir. Bu nedenle, kalp hastalıkları tedavisinde CaMKII’nin inhibisyonunu hedefleyen stratejiler geliştirilmiştir.
İskelet Kası ve Diğer Dokular
CaMKII, iskelet kası hücrelerinde de kalsiyum ile ilişkili kasılma süreçlerinde görev alır. Aynı zamanda, bağışıklık sistemi hücrelerinde CaMKII’nin işlevi, inflamatuar yanıtların düzenlenmesi ve hücresel stres sinyallerinin yönetilmesi açısından önemlidir. Bu geniş biyolojik fonksiyon yelpazesi, CaMKII’nin çok yönlü bir düzenleyici protein olduğunu ve çeşitli hastalık süreçlerinde terapötik bir hedef olarak değerlendirilmesini mümkün kılmaktadır.
Son yapılan araşatırmalarda Bilim insanları, CaMKII molekülünün nöronların saniyeler içinde bilgi kodlamasına yardımcı olduğunu keşfetti, bu öğrenmede önemli bir süreçtir. Bu, CaMKII’nin sinaps-spesifik esnekliği nasıl etkilediğine dair önceki inançlara meydan okuyor.
Nature dergisinde yayımlanan Max Planck Florida Nörobilim Enstitüsü’nden yeni bir araştırma , nöronların öğrenme süreciyle uyumlu zaman ölçeklerinde bilgiyi nasıl kodladığına dair kritik bir adımı ortaya çıkardı.
Öğrenme, saniyelerden dakikalara kadar sürebilen bir süreçtir. Ancak, beynin bilgiyi nasıl kodladığına dair en iyi bilinen mekanizmalar sinirsel aktivitenin çok daha hızlı gerçekleştiği zaman dilimlerinde işler; bu süre, öğrenme sürecine kıyasla yaklaşık 1000 kat daha hızlıdır.
Bu mekanizmalar, “Hebbian plastisitesi” olarak adlandırılır. Hebbian plastisitesine göre, iki bağlı nöron, birbirlerine saniyenin yüzde biri kadar kısa bir sürede sinyal gönderdiğinde, bu iki nöron arasındaki bağlantı güçlenir. Bu kısa zaman aralığında aktif olan nöronlar, aynı bilgiyi işlemekte ve öğrenmeyi destekleyen sinaptik güçlenme meydana gelmektedir.
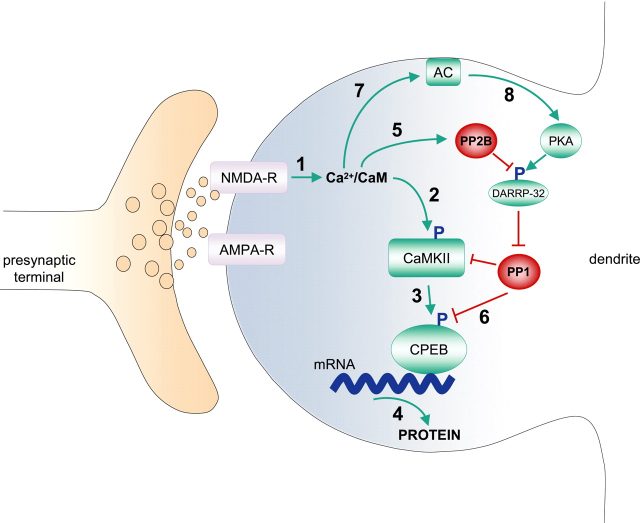
Ancak davranış sırasında bütünleştirilmesi gereken bilgiler genellikle saniyeler ila dakikalar arasında ayrılır. O zaman şu soru ortaya çıkar: Nöronlar, öğrenme ile ilişkili olan bu daha uzun zaman ölçeklerinde bilgiyi nasıl bütünleştirebilir ve kodlayabilir?
Araştırma ekibi, nöronlardaki birçok plastisite türünde kritik bir role sahip olan CaMKII molekülüne odaklandı. Dr. Jain, bu molekülün BTSP (Backpropagation-Triggered Synaptic Plasticity) süreci için önemli bir oyuncu olacağını düşündüklerini belirtti. “CaMKII’nin sinapslarda aktifleştiğini ve saniyelerce aktif kaldığını biliyorduk. Bu yüzden, nöronlarda bilgi bütünleşmesini sağlayan geniş zaman pencerelerinde anahtar bir rol oynayacağını düşündük,” dedi Dr. Jain. “Ancak, CaMKII’nin BTSP için kritik olduğu konusunda haklı çıksak da, bu molekülün işleviyle ilgili yanıldığımız noktalar oldu.”
Araştırma ekibi, CaMKII’nin işlevini bozduğunda BTSP’nin de bozulduğunu keşfetti. BTSP sürecindeki CaMKII aktivitesini görselleştirmeyi amaçlayan ekip, bu molekülün aktivitesini tespit etmek için yeni bir biyosensör geliştirdi. Önceki araçlardan neredeyse iki kat daha hassas olan bu sensörle, bilim insanları BTSP sırasında CaMKII’nin aktivitesini ölçebildiler. Ancak bekledikleri gibi bir sonuçla karşılaşmadılar.
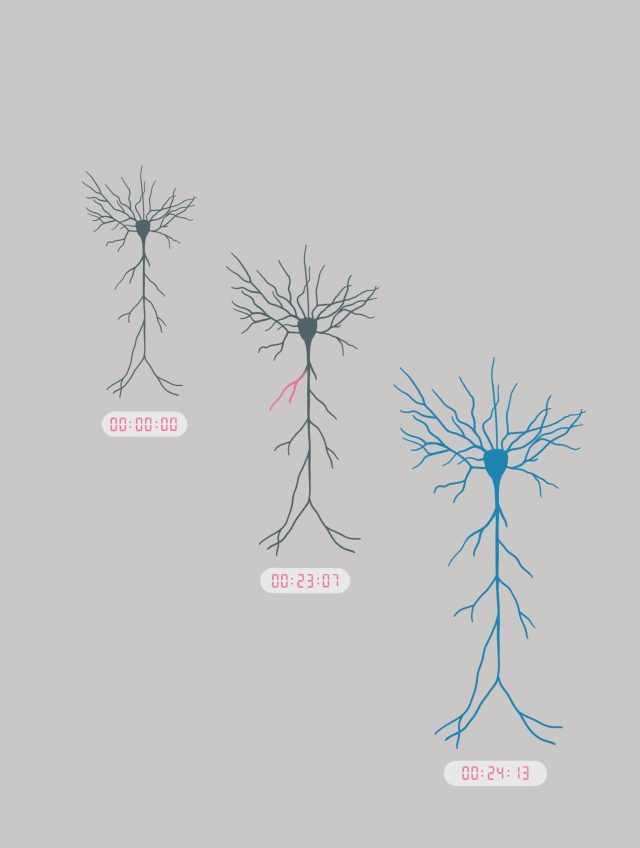
Hipotezlerinin aksine, BTSP indüksiyonu sırasında tespit edilebilir bir CaMKII aktivasyonu gözlemlenmedi. Bunun yerine, BTSP’nin başlatılmasından onlarca saniye sonra CaMKII’nin gecikmeli ve stokastik bir şekilde aktive olduğunu keşfettiler. Ayrıca, plastisite yalnızca belirli bir sinapsta gerçekleşirken, CaMKII aktivitesi nöronun çok daha geniş bir alanında görüldü. Bu bulgu, CaMKII’nin BTSP için öğretici bir sinyal sağladığını ancak sinaptik plastisitenin sinaps-spesifikliğini tanımlamadığını ortaya koydu. Araştırma, sinaptik plastisite için geniş bir zaman penceresi öneriyor ve sinaps özgül sinyallerin onlarca saniye boyunca nasıl bütünleşebileceğine dair yeni bir model sunuyor.
Dr. Jain, “Bu bulgular, CaMKII işlevine dair anlayışımızda ve sinaptik esneklik mekanizmaları hakkındaki görüşümüzde bir paradigma değişimine işaret ediyor. CaMKII’nin dendrit boyunca geniş alanlarda aktif olması, esnekliğin sinaps özgüllüğünü tanımlamaktan ziyade, dendritik bilgi işlemde yer aldığını gösteriyor. Bu bulgular, sinapslardaki bilgi kodlamasının özgüllüğünü ve CaMKII aktivasyonundaki zaman gecikmesini tanımlayan mekanizmalar gibi daha birçok soruya ışık tutuyor,” şeklinde konuştu. “Bu şaşırtıcı keşifler, moleküler aktiviteyi hafıza oluşumuyla ilişkilendirme ve öğrenme ile hafıza bozukluklarına yol açan nörolojik hastalıkları önleme çalışmalarımızda önemli bir adım teşkil ediyor. Beyindeki bilgi kodlamanın davranışsal modellerini anlamak, öğrenme ve hafızanın altında yatan mekanizmalara dair daha derin bir kavrayış sunacaktır.”
Kaynakça:
“Davranışsal zaman ölçeği esnekliğinde dendritik, gecikmeli, stokastik CaMKII aktivasyonu” Anant Jain, Yoshihisa Nakahata, Tristano Pancani, Tetsuya Watabe, Polina Rusina, Kelly South, Kengo Adachi, Long Yan, Noriko Simorowski, Hiro Furukawa ve Ryohei Yasuda, 9 Ekim 2024, Nature .
DOI: 10.1038/s41586-024-08021-8
Yazar: Tuncay BAYRAKTAR
Benzer Yazılar
Yorumlar kapatılmıştır.





